记者:其他疫苗使用26或5型腺病毒。而俄罗斯疫苗两种都使用了。您能否更具体地说明其工作原理?
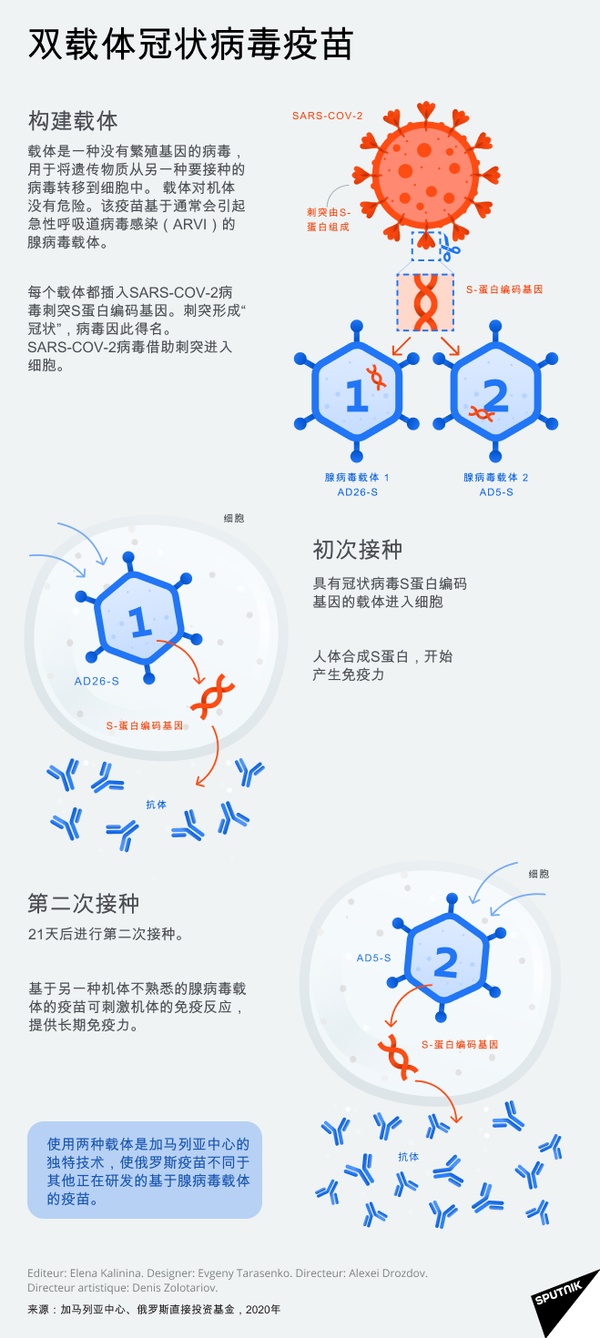
洛古诺夫:在季节性疫苗接种中,您注射一次疫苗,然后注射第二,第三次,依此类推。为什么要这样做?为了不仅形成高免疫力的反应,而且还要形成可靠的免疫记忆。首次注射药物后,将形成包括载体在内的免疫反应。如果您在第二次接种中引入相同的载体,那么已经形成的免疫力将降低疫苗接种的有效性。因此,您很难注意到免疫系统会携带所需要的基因并形成对靶抗原的免疫反应。
记者:第三阶段将有多少人参加?
洛古诺夫:最终数字还有待商定,但我可以说,将有大约3万到4万人参加。一是将有2千人参与临床试验以评估免疫原性参数,而28000志愿者将参与观察性研究以评估流行病学有效性。
每个试管都用QR码编码。将有一个应用程序,用于严格记录所有医院中的疫苗使用情况,并记录志愿者中的所有不良反应。每个接受过疫苗接种的志愿者都可以在申请中报告自己的健康状况。
记者:临床试验的不同阶段之间有何不同?
洛古诺夫:第一阶段是安全评估阶段,很少以其纯粹的形式进行。最多20人可以参加。在研究疫苗的环境中,仅对志愿者进行安全性测试而不抽血并立即查看免疫原性是一个相当愚蠢的主意。因此,第一阶段通常与第二阶段结合进行,不仅要评估安全性,还要评估有效性。在此阶段,疫苗的有效性通过其免疫原性来评估。在第三阶段,评估流行病学有效性。
我还要补充一点,如果没有成功完成强制性的临床前研究计划,就无法开始临床试验。这些是对动物安全性和免疫原性的广泛研究,没有这些研究,您将无法转向人类。同时,例如FDA(美国食品药品监督管理局,药品流通领域的美国主要监管机构)表示,经过充分研究的平台技术可以走特殊的缩短了的临床前测试程序。尽管我们对平台进行了充分的研究,但我们已经成功完成了对两种灵长类动物、兔形目动物、小鼠、大鼠、豚鼠和仓鼠的临床前研究。这里我们没有走FDA的程序。我不知道强生公司,摩纳哥公司,阿斯利康公司是否走这条程序。
记者:为什么第三阶段的研究会在临时注册后进行?
洛古诺夫:临时注册的想法和目的是使危险人群能够使用疫苗,从而保护人们免受感染或死亡的严重后果。同时,疫苗的民用推广将在严格控制下进行,这种临时登记可以随时中止。
第三阶段的目的是在随机对照试验中,对疫苗在大量志愿者身上的安全性和有效性进行大规模评估。这对于获取大量统计数据是必需的。另外,该阶段对于决定疫苗的永久注册也是必要的。
“卫星-V”是一种双载体疫苗,注射两次才能获得稳定的免疫力。第一次是注射携带新冠病毒S蛋白编码基因的载体,它可以渗入细胞中;第二次注射是加强接种,以产生更多的抗体。


 京公网安备11010502053235号
京公网安备11010502053235号